
临床开发
临床开发策略
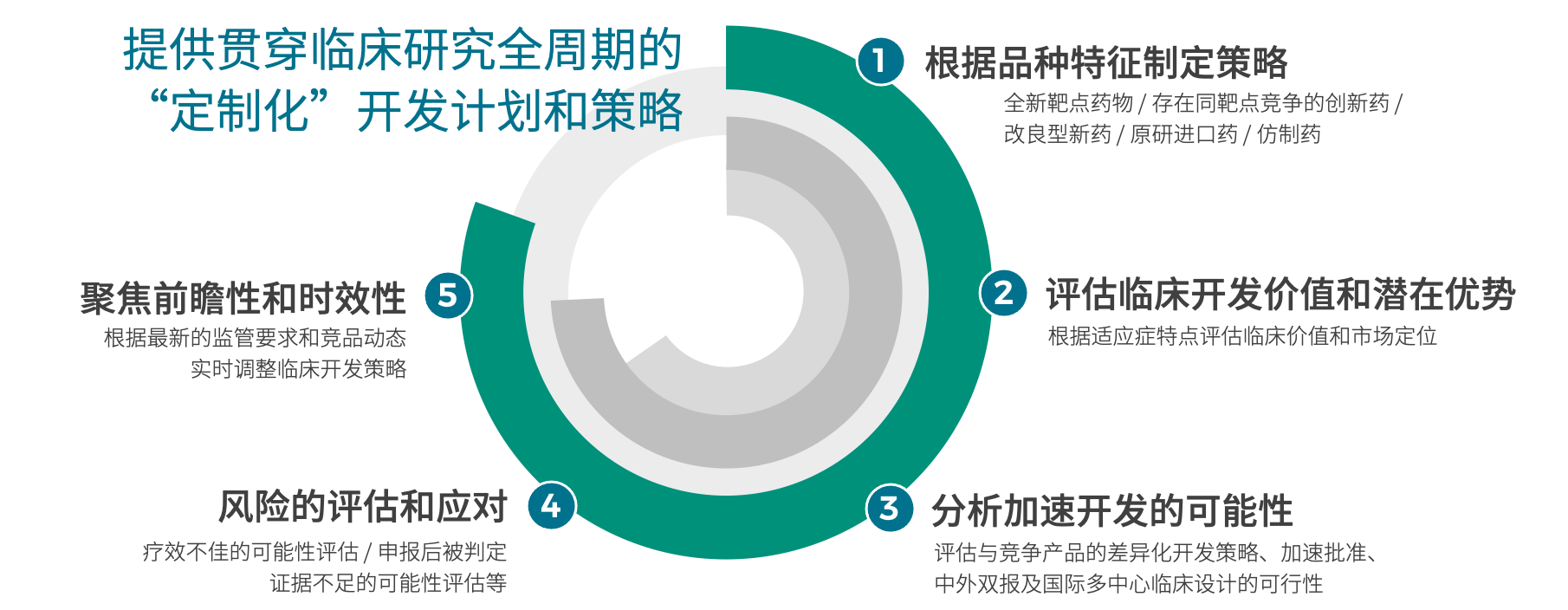
提供贯穿临床研究全周期的“定制化”开发计划和策略。
让您的产品开发更具竞争力
我们通过17年的项目经验来协助申办方设计一个完整的、可贯穿全周期的临床开发策略——以品种特征与注册申报目标为基础的“个性化”临床研发计划和方案设计服务。
全新靶点的药物
对于全新靶点的first-in-class创新药,我们将依据作用机制和临床前研究结果制定整体研发策略,包括提供目标适应症选择、从I期到II期概念验证试验的临床研发计划和方案关键要素设计、首次人体试验剂量确定、试验中和试验后的药代/药效结果解读、后期试验剂量选择和给药方案推荐、II期方案设计和加速审批的可行性分析。

存在同靶点竞争的1类创新药
对于存在同靶点竞争的1类创新药,我们将基于前期研究结果对在研产品进行潜在的优劣势分析,为产品在未来的市场定位提供建议;借鉴同类药研究情况优化当前临床研发计划和方案,缩短研发时间,降低研究成本;或者结合市场竞争局面,探索差异化开发的路径。

改良型新药
对于改良型新药,我们将依据产品的改良特征和原研药的临床应用情况,分析改良产品与未满足临床需求间的关系,以此制定临床研发计划。基于原研药已知的临床药理学特征和量效关系,制定改良品种的临床药理学研究方案,并论证是否可能减免临床疗效与安全性试验。

原研进口药
对于原研进口药,我们将依据适应症特点,结合临床实践和临床药理学研究数据撰写跨地区人群桥接分析报告。

3类仿制药
对于3类仿制药,我们将结合原研药的产品信息和获批的适应症,探索豁免临床试验的可能性或制定桥接试验及以中国患者为研究对象的临床试验方案。

制定临床开发策略时的关注要点
我们的优势
拥有医学、药理学和临床药理学等多个医药相关领域专家,可提供早期临床研发试验设计、临床药理学研究的试验设计
拥有专业的临床策略咨询顾问团队,凭借丰富的项目经验提供指导临床开发策略和监管机构沟通服务
拥有临床研究PI和CDE审评经验的重磅专家对项目进行把关
背靠泰格医药一站式服务平台,通过高效的内部交流,短时间内提供最佳的解决方案
丰富海外临床试验方案设计经验
本网站使用Cookies以使您获得最佳的体验。为了继续浏览本网站,您需同意我们对Cookies的使用。想要了解更多有关于Cookies的信息,或不希望当您使用网站时出现Cookies, 请阅读我们的Cookies声明。